2.1.2.- Las moléculas
Los átomos no suelen encontrarse libres en la naturaleza; no suelen estar solos, sino en compañía de otros átomos, formando moléculas.
Una molécula es una combinación de dos o más átomos que se mantienen fuertemente unidos.
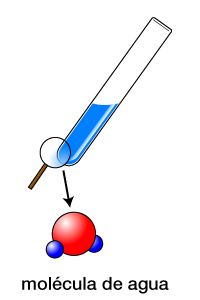
Imagen: wikimedia commons
Los átomos son como las letras del abecedario, pueden ir solos, letras sueltas (aunque es raro) o juntarse y formar palabras, nuestras moléculas, e incluso juntarse moléculas y formar "las frases de la materia".Cogemos 3 átomos de esto, 2 de aquello y... ya tenemos una molécula.
Eso sí, todas las moléculas de una determinada sustancia son exactamente iguales, y diferentes a las de todas las demás sustancias.
Por ejemplo si un átomo de oxígeno se junta con dos átomos de hidrógeno, ya tenemos una molécula de agua.
En un vaso de agua hay millones de estás moléculas; todas igualitas, todas con su átomo de oxígeno y sus dos átomos de hidrógeno.
Aunque parezca mentira, toda la materia que nos rodea, los millones de sustancias distintas que hay a nuestro alrededor, está formada por moléculas que, a su vez, se forman combinando en distintas cantidades los 92 tipos de átomos diferentes que hay.
Para representar las moléculas de forma sencilla los científicos usan los símbolos de los átomos que las forman y unos numeros que indican cuántos átomos de cada clase "entran en el juego", forman parte de esa molécula.
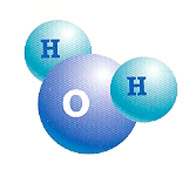
Así la molécula de agua que antes "formamos" se representa como H2O, dos hidrógenos y un oxígeno.
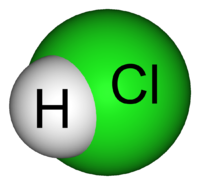
La molécula de ácido clorhídrico (salfuman o agua fuerte), está compuesta por un átomo de cloro y otro de oxígeno: HCl

La molécula de bicarbonato sódico está formada por un átomo de sodio, uno de carbono, uno de hidrógeno y tres de oxígeno: HNaCO3
A esta manera de representrar las moléculas, usando los símbolos de los átomos que la forman y un numerito que indica cuántos átomos de cada clase intervienen en ella se le llama fórmula de la molécula.
Autoevaluación
1. La molécula de sulfato de cobre está formada por un átomo de cobre, un átomo de azufre y cuatro de oxígeno. ¿Cuál de las siguientes será su fórmula?
|
CuSO3
| |
|
CoSO4
| |
|
CuSO4
|
|
HNiO3
| |
|
HNO3
| |
|
NaNO3
|
3. Marca cuál o cuáles de las siguientes fórmulas representan moléculas.
Ni
| |
O2
| |
H2O
| |
Na
| |
Fe
| |
H2
| |
CaCO3
| |
Antes de terminar este apartado dedicado a lo muy, muy pequeño, puedes repasar lo que has estudiado si ves esta animación:
