1.- Casi siempre agua... con otra cosa pero agua.

Imagen: istockphoto
Miguel y su abuelo Mateo salen como siempre al campo por la mañana temprano a abonar un poco las plantas que son jóvenes y necesitan alimento.
–Mateo: este año el estiércol no es muy bueno, Miguel.
–Miguel: pues utiliza una disolución de nitrógeno, fósforo y potasio con agua.
–Mateo: –se ríe y le dice– eso es el 15-15-15, antes lo utilizaba, pero dejé de hacerlo.
Miguel (que se cree que su abuelo solo sabe de campo) le pide al abuelo que explique qué es eso del 15-15-15.
–Mateo: Miguel, me extraña que tú no sepas que es eso, ¡con todo lo que estudias! es el porcentaje de cada mineral en ese tipo de abono.
Incrédulo por la contestación Miguel se ríe.
–Mateo: Anda en lugar de reírte ¿por qué no preparas las máquinas? ¿sabes lo que es el soluto y el disolvente? ¿no? pues recuérdalo y no te rías de tu pobre abuelo.
¿Qué te parece si lo recordamos?
En el tema anterior viste que la disolución es una mezcla homogénea de varios componentes: soluto y disolvente, soluto es el que se encuentra en menor cantidad mientras que el disolvente es el que está en mayor cantidad y determina el estado de la disolución (sólido, líquido y gaseoso).
Repasa la diferencia entre soluto y disolvente en la siguiente animación:
El agua es el disolvente universal, es decir disuelve a casi todas las sustancias. ¿Quieres ver como lo hace? si pinchas en la molécula de agua lo verás claro, aunque también lo puedes ver con este otro ejemplo
Esto permite, por ejemplo, que los vegetales puedan incorporar minerales disueltos en el agua y a los animales les facilita la circulación por la sangre de desechos y nutrientes.
¿Sabías que son muy distintas cuando se disuelven?
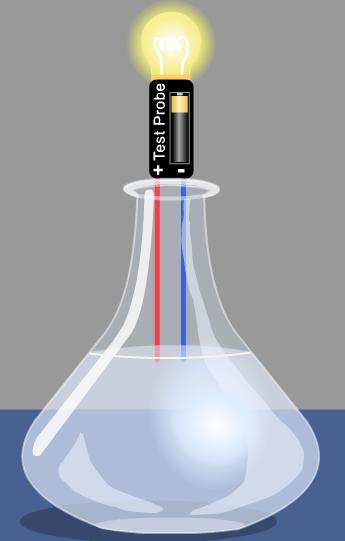
Imagen: NCSSM
No todas las sustancias se comportan de la misma manera en el agua, por ejemplo la sal y el azúcar, cuando las disolvemos en agua, aparentemente son iguales, podríamos confundirlas, sino fuera por su sabor distinto, sin embargo, son moléculas distintas, que en el agua de comportan de distinta forma, si lo quieres ver, pincha en las siguientes animaciones:
Has visto que la sal en agua conduce la electricidad, por eso se dice que es un electrolito, porque en disolución se separa la molécula en sus iones (átomos con carga recuerdas), mientras que el azúcar no es un electrolito, no se separan sus átomos en agua (no se forman iones) por lo que no conducen la electricidad.

Imagen: dreamstime
- ¿Qué ocurre si te pasas con el azúcar en el café? ¿A que no sabe bien?
- En el cuerpo humano, por ejemplo, la sangre siempre debe tener unos determinados niveles de azúcar (glucosa), y prácticamente de todos los componentes (colesterol, potasio, hierro...)
- Las bebidas también han de tener una proporción adecuada de sus componentes para conservar el mismo sabor.
Cuando preparamos una disolución, nos interesa conocer en qué proporción se encuentran el soluto y el disolvente. A esa proporción los científicos la conocen como concentración de la disolución.
La concentración de una disolución indica la cantidad de soluto que hay en una cantidad determinada de la disolución.
La concentración de una sustancia la podemos expresar de muchas formas, vamos a ver algunas de ellas:
El porcentaje en masa nos indica los gramos de soluto que hay en 100 g de disolución.
¡¡No olvides que los gramos de disolución son los gramos del soluto más los del disolvente!!
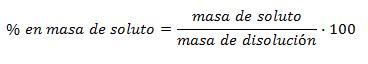

Imagen: MEC-ITE
Ejemplo
Se ha preparado una disolución añadiendo 10 g de azúcar y 5 g de sal a 100 g de agua. Calcula:
- El porcentaje en masa de azúcar.
- El porcentaje en masa de sal.
El porcentaje en volumen nos indica el volumen de soluto que hay en 100 unidades de volumen de disolución.
¡¡No olvides que el volumen de disolución es la suma del volumen del soluto más el volumen del disolvente!!


Imagen: Chemistryland.com
Ejemplo
Se ha preparado una disolución añadiendo 10 ml de alcohol a 100 ml de agua.
Calcula el porcentaje en volumen de alcohol.
¿Sabes la cantidad de alcohol que tomamos cuando bebemos…?
| Bebida | Porcentaje de alcohol en volumen |
| Cerveza | 3,5-5 |
| Sidra | 4 |
| Vino | 10-15 |
| Cava | 12 |
| Vino dulce | 15-22 |
| Vermut | 16-24 |
| Pacharán | 28 |
| Whisky | 35-40 |
| Anís | 40 |
| Ron, Vodka | 40 |
| Absenta | 60-80 |
¿Qué tiene más alcohol, 3 tercios de cerveza o un whisky (100 ml)?
- Un litro de cerveza (3 tercios) como tiene entre 3,5 y 5 ml por cada 100 ml, un litro tendrá entre 35 y 50 ml de alcohol.
- 100 ml de whisky tiene 35 y 40 ml de alcohol. Pues para que veas, es más o menos lo mismo.
Si tenemos una disolución de una sustancia en agua, podemos añadir soluto y remover hasta que se disuelva. Pero llega un momento en que no se puede disolver más y cualquier cantidad adicional de soluto se queda depositada en el fondo del recipiente.
A la cantidad máxima de soluto que se puede disolver en un cantidad de disolvente determinada se le llama solubilidad y se expresa en g de soluto/ L de disolvente.
Cuando una disolución no admite más soluto se dice que está saturada, sino está saturada pero le falta poco para estarlo se dice que está concentrada y si le falta mucho se dice que está diluida, como verás en la siguiente animación, en la que diluimos una disolución al añadir más disolvente.

Imagen: flickr.com / Takashy
Para saber más…
Si quieres un buen vaso de colacao sin grumos, deberás calentar la leche ¿sabes por qué?
Pues porque al aumentar la temperatura la mayoría de las sustancias se disuelven mejor. En el siguiente enlace podrás ver otros casos curiosos relacionados con la solubilidad:
También podrás comprobar en un test animado que esto es cierto, que la velocidad de disolución aumenta con la temperatura.
Autoevaluación
Preparamos una disolución que contiene 2 g de cloruro sódico conocido como sal común, (NaCl) y 3 g de cloruro de potasio (KCl) en 100 g de agua destilada. Halla el tanto por ciento en masa de cada soluto en la disolución obtenida.
|
1,9 % de NaCl y 3,6 % de KCl
| |
|
5,9 % de NaCl y 2,8 % de KCl
| |
|
1,9 % de NaCl y 2,8 % de KCl
|